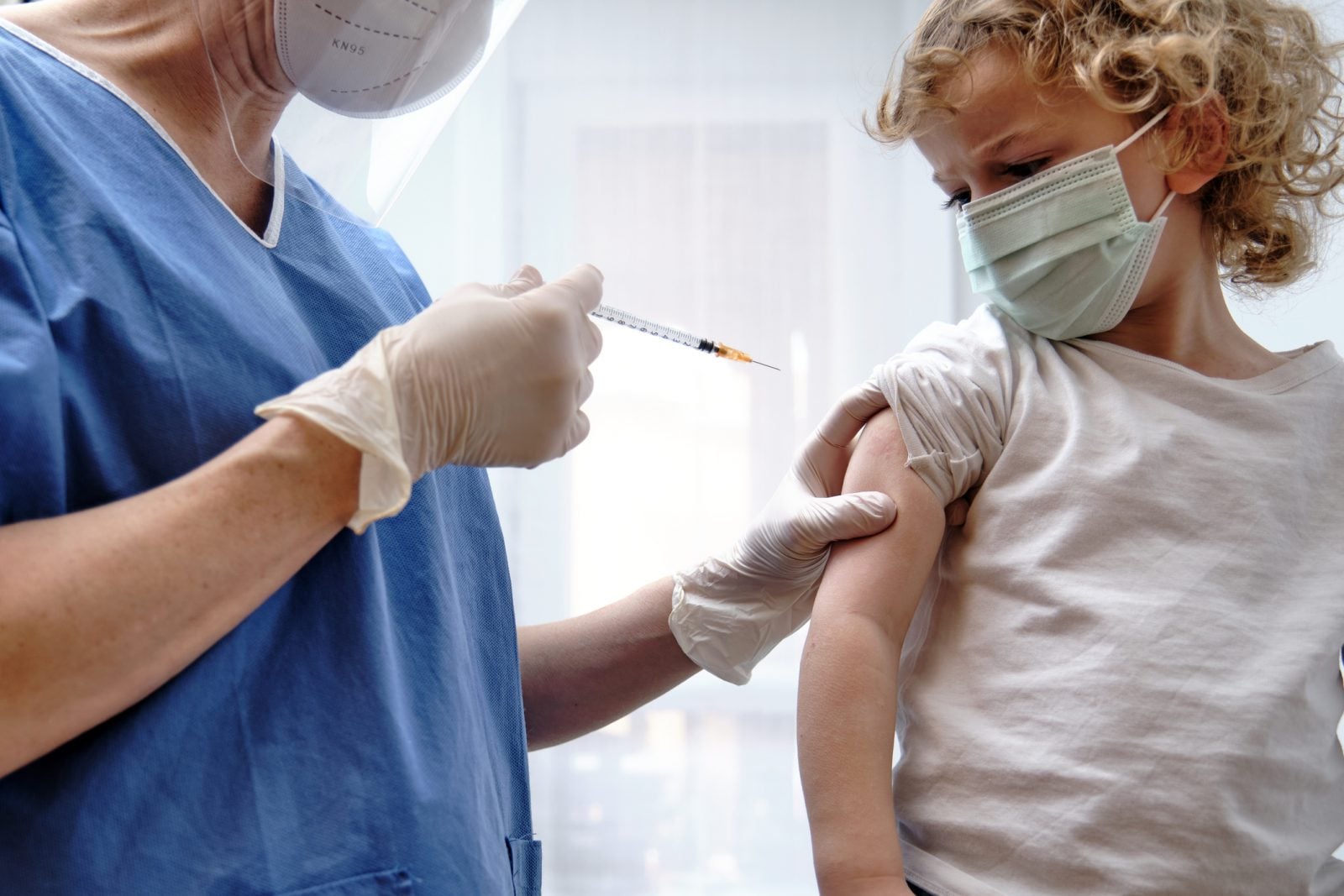
W pierwszym etapie badań https://www.focus.pl/artykul/szczepionka-moderny-na-sars-cov-2-jako-druga-skuteczna-ponad-90-proc przetestuje, jak dzieci reagują na różne poziomy dawek szczepionki. Firma podała, że dzieci w wieku powyżej 2 lat mogą otrzymać 50 lub 100 mikrogramów szczepionki na dawkę, podczas gdy dzieci w wieku poniżej 2 lat mogą otrzymać 25, 50 lub 100 mikrogramów.
Każde dziecko biorące udział w testach otrzyma dwie dawki szczepionki, przy czym druga dawka zostanie podana po 28 dniach od pierwszego zastrzyku. Odstęp między dawkami jest taki sam, jak w przypadku dorosłych.
Pierwsze ze szczepione dzieci w każdej grupie wiekowej otrzymają najniższą przewidywaną dawkę, aby można było zaobserwować ewentualne skutki uboczne przed podaniem wyższych dawek kolejnym dzieciom – opisuje przebieg testów The New York Times.
Po pierwszym etapie badań Moderna przeprowadzi analizę okresową, aby określić, który poziom dawki jest odpowiedni dla każdej grupy wiekowej. Dzieci zakwalifikowane do drugiego etapu badania otrzymają albo dawkę wybraną w analizie, albo placebo.
Wszyscy uczestnicy badania będą monitorowani przez rok po zaszczepieniu, aby prześledzić występowanie możliwych skutków ubocznych, ocenić poziom przeciwciał przeciw koronawirusowi (i trwałość ochrony poszczepiennej) oraz przypadków zakażenia COVID-19. Opierając się na tych danych Moderna będzie mogła podać, jak skuteczną ochronę daje szczepienia w przypadku niemowląt i małych dzieci.
Do użytku trafi w 2022 roku
Szczepionka Moderna, zwana mRNA-1273, nie zawiera samego koronawirusa i nie może powodować COVID-19. Zamiast tego zawiera cząsteczkę zwaną mRN przenoszącą informacje o budowie białka kolca wirusa SARS-CoV-2 wywołującego chorobę. Po wejściu do organizmu zaszczepionej osoby mRNA „mówi” komórkom, aby zbudowały białko kolca, co pozwala układowi odpornościowemu rozpoznawać to białko i wykształcić odpowiedź immunologiczną. W ten sposób organizm zaszczepionej osoby jest chroniony przed wirusem.
– Jesteśmy podbudowani wstępną analizą badania fazy 3 COVE mRNA-1273 u osób dorosłych. Badanie pediatryczne pomoże nam ocenić potencjalne bezpieczeństwo i immunogenność naszego kandydata na szczepionkę w młodszej populacji – mówi Stéphane Bancel, dyrektor generalny Moderny.
Moderna szacuje, że w badaniu dzieci i niemowląt udział weźmie 6750 uczestników. Firma prowadzi obecnie badania wśród 3000 dzieci w wieku od 12 do 17 lat. To badanie obejmuje również rok obserwacji i zostanie prawdopodobnie zakończone w czerwcu 2022 r.
Szczepionka mogłaby potencjalnie zostać dopuszczona do stosowania w nagłych wypadkach u dzieci przed upływem tego okresu, ale nie wiadomo, kiedy i czy to się stanie – podkreśla Times.